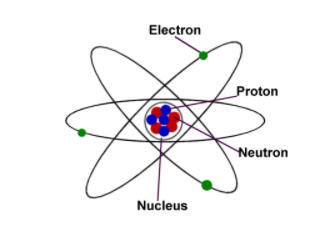
我们周围的世界由称为原子的微小物质组成。这些原子如何粘在一起形成物质称为化学键。

关于原子
每个元素都有其自己的独特原子,该原子由原子核中特定数量的质子组成,称为原子数。每个原子也具有与其质子相同的电子数。
电子壳
电子围绕原子核运动。它们停留在称为壳的层中。每个壳只能包含一定数量的电子:第一层可以容纳两个电子,第二层可以容纳两个电子,第三层可以容纳十八个电子,依此类推。
外壳
所有原子都想拥有一个完整的外壳,但是自然拥有一个完整的外壳的唯一元素是元素周期表右侧的稀有气体。结果,当没有完整外壳的原子与其他原子接触时,它们趋向于放弃或获得电子。
价电子
价电子是原子外壳中可参与与其他原子形成化学键的电子数。
具有相对空的外壳的原子将要放弃电子。例如,如果一个原子在其外壳中可能有8个电子中有1个电子,它将希望放弃该电子,因此其外壳现在已满。
具有相对完整的外壳的原子将希望获得电子以填充外壳。例如,一个在其外壳中具有8个电子中的6个的原子将试图获得2个电子,因此其外壳是充满的。
离子键
合当一个元素向另一个元素提供电子时,就会发生离子键合,从而两个元素都具有完整的外壳。
示例:
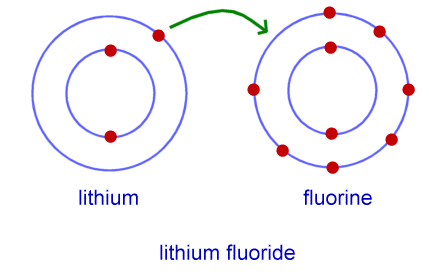
这是一个示例,显示锂(在外壳中具有3个电子和1个电子)和氟(在外壳中具有9个电子和7个电子)给电子以形成LiF或氟化锂。这称为离子键。
共价键
在共价键中,电子是在原子之间共享的,而不是给电子,是为了使两个元素的原子都获得完整的外壳。电子总是成对共享。
例子:
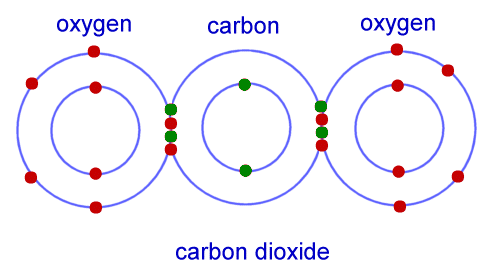
共价键的例子是二氧化碳分子。在该示例中,碳在其外壳中具有8个电子中的4个,氧具有8个电子中的6个。通过将两个氧原子与一个碳原子结合,原子可以共享电子,从而每个原子都具有完整的外壳。
关于化学键的有趣事实
因为稀有气体具有自然充满的外壳,所以它们很少发生反应。
在金属键中,大量原子失去电子。
离子键主要形成在位于元素周期表左侧的金属之间。
分子中的原子通过原子核和共享电子之间的吸引力保持在一起。